【大紀元2021年02月04日訊】(大紀元記者江禹嬋台北報導)治療癌症時最大的困擾是抗藥性。台灣陽明交通大學生科院結構生物學團隊,為了解決抗藥性問題,解析APE1蛋白質與DNA的複合物結構,可損壞癌細胞的DNA,讓抗癌藥物進行有效的治療。
此外,通常癌細胞會用APE1的DNA來修復,未來可望利用結構基礎藥物設計,阻斷APE1的活性,就有助於解決部分癌細胞的抗藥性問題。
許多藥物在冶療初期能有效用,但隨著治療時間愈久,藥物開始失效,醫學上稱此現象為抗藥性。例如抗生素殺菌的效果越來越低,甚至失效,原因是未被殺死的細菌,在繁殖過程中不斷變異來適應藥物以求生存。
治療癌症的藥物也有相同現象,患者服用初期,腫瘤生長或許能被有效抑壓,但經過一段時間後,腫瘤會再度生長。
陽明交通大學4日表示,此項研究由分子醫學與生物工程研究所副教授蕭育源主導,與生物資訊及系統生物研究所教授朱智瑋合作,研究生劉東璋、林俊廷、郭鎧瑋與大學專題生張楷成共同執行,研究成果已刊登在國際期刊《自然通訊》(Nature Communications)。
研究團隊指出,APE1蛋白質有氧化還原、DNA內部剪切及DNA外側剪切能力,部分抗癌藥物可損壞癌細胞的DNA,或嵌入癌細胞的DNA,藉此阻斷DNA複製來殺死癌細胞。
不過癌細胞也可能利用APE1的DNA修復能力,以及外側剪切能力,來修補癌細胞的DNA或移除嵌入DNA中的抗癌藥物,導致部分抗癌藥物失效。
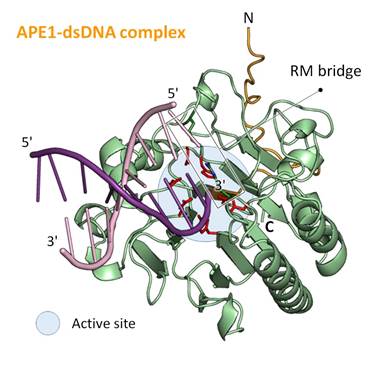
因此研究團隊利用X-ray蛋白質晶體學方法,解析出數種APE1與DNA複合體結構,搭配酵素活性分析,系統性建構出APE1的DNA外側剪切活性分子機制。
此舉可釐清APE1蛋白質如何剪切DNA,未來可依APE1的蛋白質結構開發小分子抑制劑,阻斷APE1的活性,有助於解決部分癌細胞的抗藥性問題。
由於陽明大學與交通大學兩校合併,蕭育源表示,除了年輕學者養成計劃為主要經費支持之外,由陽明交通大學的生物科技學院所提供的硬體,如新落成的生醫大樓賢齊館,以及陽明交通大學兩個研究中心所提供的研究鍵結與儀器設施更是促成此研究成果的主要推手,相信合校後的陽明交通大學一定會有更良好的研究產出。

責任編輯:高靜 #






