【大纪元2022年09月22日讯】(大纪元记者林慧真香港报导)感染COVID-19会导致肺脏内形成血栓,严重时可能致命,也有引发严重后遗症的风险。台湾中研院一项研究发现COVID-19患者发生血栓的关键原因,COVID-19病原体SARS-CoV-2会活化血小板以放大发炎反应,进而产生血栓。只要阻断嗜中性白血球表面的两个受体CLEC5A和TLR2,就可以缓解血栓症状并且减少血管内凝血以及发炎。
研究报告的第一作者、基因体研究中心博士后研究学者宋佩珊表示,收集COVID-19急性期患者的血液样本发现,血液中含有高量的胞外囊泡(EV),这些囊泡大多来自血小板,显然与血小板遭遇病毒之后被活化有关。当血小板被病毒激活后,释放大量胞外囊体刺激嗜中性白血球,产生大量的嗜中性白血球胞外网状结构(NETs)及自杀式细胞死亡(NETosis)。早前研究已经发现,虽然NETs形成有助于清除病菌,但过多NETs会引发血栓,导致肺部微血管阻塞。
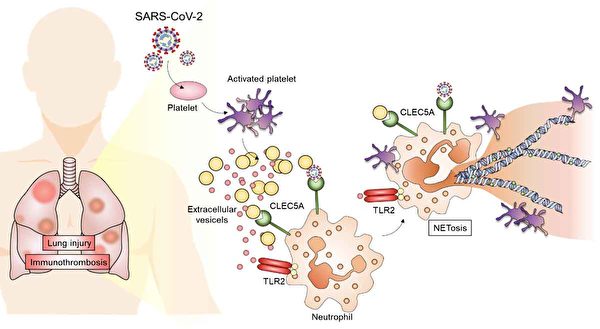
研究团队分别采取健康受试者、COVID-19病人的胞外囊泡进行质谱仪分析,发现,SARS-CoV-2感染引起的胞外囊泡表现大量血小板相关蛋白,且具有多种与白血球去颗粒性及血小板活化凝集的蛋白,显示COVID-19病人血液中血小板剧烈活化。
研究团队进一步将健康人和COVID-19病人的胞外囊泡与嗜中性白血球培养,结果显示健康对照组的胞外囊泡无法诱导NETs形成,但COVID-19病人的胞外囊泡诱导了强大的NETs形成,而阻断嗜中性白血球表面的两个受体CLEC5A和TLR2,能够抑制NETs形成。
在动物实验中,研究人员发现,小鼠感染SARS-CoV-2病毒3至5天后,肺部会产生大量的NETs以及严重的细胞浸润;而对于CLEC5A和TLR2基因剔除的小鼠,发炎以及细胞浸润的情况大幅降低。
中研院基因体研究中心特聘研究员谢世良指出,CLEC5A和TLR2是有希望的治疗靶点,可在未来减轻血栓炎症,并降低产生COVID-19后遗症的风险。
研究已发表在《Journal of Biomedical Science》期刊。@
责任编辑:陈玟绮