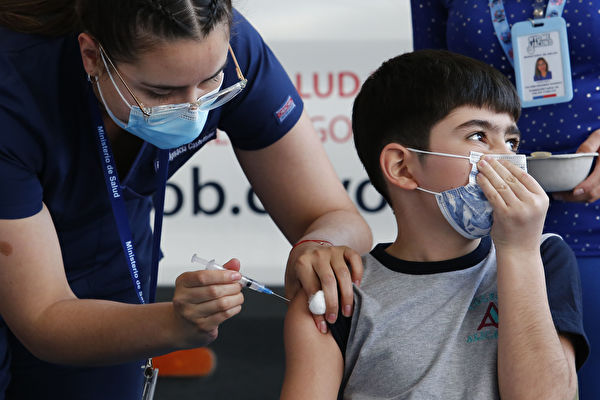
【大纪元2022年02月12日讯】(英文大纪元记者Zachary Stieber报导/高杉编译)美国药品监管机构周五(2月11日)宣布,他们决定推迟授权辉瑞公司COVID-19疫苗用于年仅6个月至4岁的幼儿。
美国食品和药物管理局(Food and Drug Administration,简称FDA)原计划在2月15日就幼儿接种COVID-19(中共病毒)疫苗问题咨询其顾问委员会,并可能在该咨询会议召开后的数小时内,就发布紧急使用授权(EUA)。但是,鉴于对辉瑞公司2月1日发送的初步数据的评估,这个计划已经发生变化。
食品和药物管理局官员现在认为,他们尚不能批准为6个月到4岁的儿童接种疫苗,他们还需要从一项正在进行的、针对该年龄组的三剂量方案试验中获得相关数据。
食品和药物管理局生物制品评估与研究中心(Center for Biologics Evaluation and Research)主任彼得‧马克斯(Peter Marks)博士在电话采访中告诉《大纪元时报》(The Epoch Times)记者:“所看到的数据让我们意识到,我们还需要看一看正在进行的三剂量实验的数据,之后才能确定我们可以对之进行授权。”
他补充说:“我认为,家长们可以放心,我们已经制定了一个标准,如果达不到这个标准,我们就不会继续下去。”
在周五发布声明之前,多名顾问小组成员拒绝了采访请求。《新英格兰医学杂志》(New England Journal of Medicine)主编埃里克‧鲁宾(Eric Rubin)博士是该小组的成员之一,他在一封电子邮件中告诉《大纪元时报》(Epoch Times):“目前很难得出任何结论”,因为成员们还没有看到数据。
目前,每个5岁以上的美国人都可以接种辉瑞公司的两剂量疫苗。
2021年12月,辉瑞公司和它的合作伙伴BioNTech公司宣布,在幼儿身上进行的测试显示,两剂量的疫苗使6个月到1岁的幼儿产生了足够的免疫反应;但对2到4岁的儿童没有效果。他们当时表示,他们计划为这个年龄段的孩子测试一种三剂量的接种方案。
但不久之后,因为担心COVID-19确诊感染病例数量和所有年龄组的住院人数激增,美国食品药品监督管理局要求这些公司提供相关数据。2月1日,辉瑞公司和BioNTech公司要求为该年龄段的孩子申请紧急使用授权。
在疫情爆发至今,尤其是因Omicron变异体引发的感染,很少有儿童因感染病毒导致了严重疾病或死亡。但是,一些家长和健康组织仍一直在向食品和药物管理局施压,要求该机构批准针对幼儿的疫苗接种。他们认为,这样做将有助于保护孩子们免受感染,以及可降低因此导致的住院治疗及死亡率。
但批评人士指出,辉瑞公司生产的疫苗和其它两种获准在美国使用的疫苗,在面对较新的变异体菌株,尤其对Omicron变异体菌株时,有效性已经大幅下降。与此同时,疫苗却有带来副作用的风险。所以,不值得让年幼的儿童去接种疫苗。
责任编辑:叶紫微#